Chapitre III
La microencapsulation
III.1.Historique :
Les premières publications sur la microencapsulation et
ses applications possibles dans le domaine pharmaceutique remontent à
1931.De 1931 à 1940, GREEN et son équipe à la NCR (USA)
ont établi un processus de microencapsulation basé sur
l'utilisation d'une enveloppe de gélatine (coacervation)
(Anonyme 8).
Depuis lors, l'industrie pharmaceutique a
développé plusieurs autres matériaux de revêtement
et beaucoup d'autres méthodes d'encapsulation.
Dans les 30 années, plusieurs brevets ont
été enregistrés au sujet de l'encapsulation des PA,
médicinaux et non médicinaux, comme des antibiotiques, vitamines,
et ainsi de suite.
D'autres industries ont été
intéressées, et le sont toujours, par cette technique :
l'industrie alimentaire, l'industrie photographique, l'industrie des engrais,
l'industrie de pesticides, etc.
En outre, l'industrie chimique avait développé
de nouveaux polymères avec des applications potentielles dans la
microencapsulation (Chang et Prakach, 2001).
III.2. Définition :
La microencapsulation regroupe l'ensemble des technologies qui
permettent la préparation de microparticules individualisées,
constituées d'un matériau enrobant contenant une matière
active.
- Les matériaux enrobants sont des polymères
d'origine naturelle ou synthétique, ou des
lipides.
- Les matières actives sont d'origines très
variées: principes actifs pharmaceutiques, actifs cosmétiques,
additifs alimentaires, produits phytosanitaires, essences parfumées,
microorganismes, cellules, ou encore catalyseurs de réaction chimique
...etc.
Les microparticules présentent une taille comprise
entre environ 1um et 1mm et contiennent typiquement entre 5 et 90 % (en masse)
de matière active (Richard et Benoit, 2000).
III.3. Types de microparticules :
Les procédés de microencapsulation permettent de
préparer des microparticules de deux types: (fig.12)
- Les microcapsules, la particule réservoir est
constituée d'un coeur de matière active liquide (plus ou moins
visqueux) ou solide, entourée d'une écorce solide continue de
matériau enrobant. Les microcapsules ne sont pas nécessairement
sphériques ;
- Les microsphères, un réseau
macromoléculaire ou lipidique continu formant une matrice dans laquelle
se trouve la matière active finement dispersée, à
l'état de molécules, de fines particules solides ou encore de
gouttelettes de solutions (Richard et Benoit, 2000).
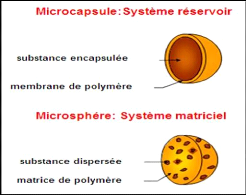
Figure (12) : Types de
microparticule (Anonyme 9).
Un certain nombre de facteurs physico-chimiques, permettent de
caractériser la membrane d'une microcapsule ou la matrice d'une
microsphère :
- Charge électrique de surface ;
- Mouillabilité ;
- Porosité ;
- Tortuosité des pores ;
- Degré de gonflement.
Le taux d'encapsulation (ou la teneur en matière
active) peut être très élevée dans les
microcapsules, de l'ordre de 85 à 90 % (rapport massique).
Comparés à ceux rencontrées dans les microsphères
qui sont plus faibles, de l'ordre de 20 à 35 % (Richard et
Benoit, 2000).
Le rendement d'encapsulation est le rapport entre la masse de PA
encapsulé et la masse de PA à encapsuler (Anonyme
9) :
× 100
Masse de PA à encapsuler
Rdt=
Masse de PA encapsulé
III.4. Intérêt de microencapsulation
:
Sur le plan industriel, la microencapsulation est mise en oeuvre
pour remplir les objectifs suivants :
- Assurer la protection, la compatibilité et la
stabilisation d'une matière active dans une formulation ;
- Réaliser une mise en forme adaptée (dosage plus
élevé dans de petits volumes) ; - Améliorer la
présentation d'un produit ;
- Masquer un goût ou une odeur ;
- Modifier et maîtriser le profil de libération
d'une matière active pour obtenir, par exemple, un effet prolongé
ou déclenché (Richard et Benoit, 2000).
III.5. Procédés de microencapsulation
:
Avant de procéder une préparation d'une
microencapsulation, il faut tenir compte : - La taille moyenne et la largeur de
distribution granulométrique;
- La teneur en matière active ou taux d'encapsulation ;
- La forme finale: dispersion de microparticules en phase aqueuse
ou en phase solvant, poudre sèche ;
- Les contraintes de stabilité au cours du stockage et au
cours de la mise en oeuvre ;
- La durée de conservation sans libération de
matière active, ainsi que le milieu dans lequel les particules seront
conservées ;
- Les conditions de libération et la cinétique
de libération. Si l'on souhaite une libération
déclenchée, il devra en particulier être
précisé quel est le paramètre de déclenchement:
pression ou cisaillement mécanique, variation de température,
variation de pH, dégradation enzymatique. Pour une libération
prolongée, la durée souhaitée de la période de
libération sera une des données du problème ;
- Les contraintes réglementaires liées au
domaine d'application et au mode d'administration qui sont prescrites dans les
réglementations nationales et internationales (Pharmacopée
Européenne ou USP par exemple, pour le domaine de la pharmacie).
Les choix du procédé et de la formulation
déterminent les caractéristiques finales de microparticules
(Richard et Benoit, 2000).
III.5.1. Procédés physico-chimiques
:
III.5.1.1. Procédé basé sur la
séparation de phase :
La coacervation est le phénomène de
désolvatation des macromolécules, conduisant à une
séparation de phases au sein d'une solution. A l'issue de la
coacervation, deux phases sont présentes dans le milieu :
- Le coacervat : Riche en polymère et pauvre en solvant
;
- Le surnageant : Pauvre en polymère et riche en
solvant.
Si, dans le même temps, une matière active est
dispersée dans ce milieu, sous forme de gouttelettes par exemple, le
coacervat formé pourra l'encapsuler si les conditions d'étalement
des phases en présence sont respectées.
La figure 13 représente trois situations possibles: Cas
où une encapsulation complète aura lieu, partielle, ou pas
d'encapsulation, (l'encapsulation est complète si le coacervat mouille
spontanément la surface de la matière active, c'est-à-dire
lorsque S3 > 0, S2 < 0 et S1
< 0) (Richard et Benoit, 2000).
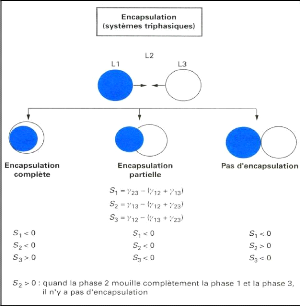
Figure (13) : Comportement d'un coacervat
(3) vis-à-vis une phase liquide
non miscible (1)
(Richard et Benoit, 2000).
III.5.1.2. Microencapsulation par coacervation
complexe :
La coacervation complexe est une désolvatation
simultanée de deux polyélectrolytes hydrosolubles portant des
charges opposées en provoquant par une modification de pH du milieu
aqueux. En effet, la structure du coacervat est complexe puisqu'elle comprend
deux polymères.
Le procédé de microencapsulation par
coacervation complexe se déroule de la façon suivante (fig.14)
:
- Dans un premier temps, le produit à encapsuler (sous
forme liquide ou solide) est dispersé dans une solution aqueuse
contenant les deux polymères (phase a).
- Dans un deuxième temps, la coacervation est induite
par un ajustement du pH de la solution, de façon que les charges
positives du premier polymère équilibrent les charges
négatives du second (phase b). L'attraction électrostatique des
deux polyélectrolytes provoque l'apparition d'un coacervat mixte.
- Dans un troisième temps, les gouttelettes de
coacervat formé viennent s'adsorber (phase c) à la surface de la
matière active à encapsuler et former un enrobage continu (phase
d). Finalement, cet enrobage est consolidé par réticulation
(phase e) des macromolécules constitutives du coacervat (Richard
et Benoit, 2000).
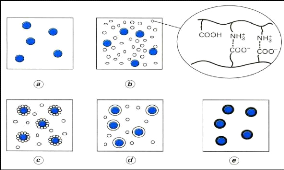
Figure (14) : Schéma de principe du
procédé de microencapsulation par
coacervation
complexe (Richard et Benoit, 2000).
Le polyélectrolyte chargé positivement qui est
généralement utilisé est la gélatine de haut point
isoélectrique (gélatine de type A telle que la gélatine de
peau de porc). Les polyanions les plus souvent utilisés sont la gomme
arabique, les alginates, les carraghénanes. La
carboxyméthylcellulose, les polyphosphates et d'autres.
Les particules obtenues sont des microcapsules. Leur taille
varie de quelques micromètres à quelques centaines de
micromètres. Les taux d'encapsulation peuvent être très
élevés, de l'ordre de 80%.
La microencapsulation par coacervation complexe est largement
utilisée dans de nombreux secteurs industriels. Dans le milieu
pharmaceutique, cette technique est également mise en oeuvre pour la
microencapsulation de paraffine liquide, d'huiles essentielles utilisées
en aromathérapie (Richard et Benoit, 2000).
III.5.1.3. Microencapsulation par coacervation simple
:
La coacervation simple se rapporte aux procédés
faisant intervenir la désolvatation d'un seul polymère par l'un
des facteurs suivants : abaissement de température, addition d'un
nonsolvant, addition d'électrolytes, addition d'un deuxième
polymère incompatible. Ce phénomène peut se
dérouler en milieu aqueux ou organique. Les étapes du
procédé sont en tous points identiques à celles
décrites pour la coacervation complexe.
Les particules obtenues sont généralement des
microcapsules. Toutefois, dans certains cas, le procédé par
coacervation simple permet d'obtenir des microsphères. C'est le cas
lorsque la proportion de substance active est faible par rapport au volume du
coacervat.
La taille des microparticules obtenues ainsi que la teneur en
matière active sont semblables à celles résultant du
procédé par coacervation complexe (Richard et Benoit,
2000).
III.5.1.4. Procédés
d'évaporation et d'extraction de solvant :
La méthode de microencapsulation par évaporation
de solvant repose sur l'évaporation de la phase interne d'une
émulsion sous agitation. Les étapes sont résumées
comme suit: Initialement, le matériau d'enrobage,
généralement un polymère hydrophobe, est dissous dans un
solvant organique volatil. La molécule active à encapsuler est
alors soit dissoute, soit dispersée dans la solution organique.
- La phase organique est émulsionnée sous agitation
dans une phase aqueuse, contenant un agent tensioactif.
- Une fois l'émulsion établie, le solvant
organique diffuse progressivement dans la phase continue sous agitation pour
s'évaporer, laissant le polymère précipiter sous forme de
microsphères (fig.15).
Ce procédé permet la fabrication de
microsphères de taille entre 0,5 et 200 um.
Le rendement de production peut aisément s'approcher de
100 % (Richard et Benoit, 2000).
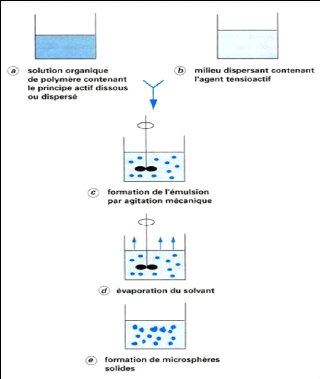
Figure (15) : Schéma de
principe du procédé de microencapsulation par évaporation
de solvant (Richard et Benoit, 2000).
III.5.1.5. Microencapsulation par gélification
thermique :
Ce procédé, encore appelé hot
melt, repose sur la fusion du matériau d'enrobage. La
matière active à encapsuler est dissoute ou dispersée dans
ce matériau fondu. L'ensemble est émulsionné dans une
phase dispersante, dont la température est maintenue supérieure
à la (Tf) de l'enrobage et pour laquelle la matière active n'a
aucune affinité: il s'agit d'eau distillée lorsque la substance
à encapsuler est lipophile, et d'huile de silicone, par exemple,
lorsqu'elle est hydrosoluble. La solidification des globules dispersés
est obtenue en refroidissant brutalement le milieu (fig.16) (Richard et
Benoit, 2000).
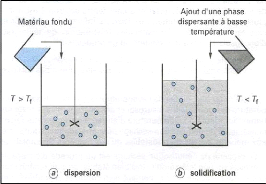
Figure (16) : Schéma de principe du
procédé d'encapsulation par gélification
thermique (hot
melt) (Richard et Benoit, 2000).
Comme de nombreuses substances actives sont thermolabiles, les
matériaux supports généralement utilisés dans ce
procédé de microencapsulation sont des lipides de bas point de
fusion. Les particules obtenues sont ici des microsphères d'une taille
pouvant aller généralement de 30 à 300 um. La teneur en
matière active est de l'ordre de 20 % (Richard et Benoit,
2000).
III.5.2. Procédés mécaniques
:
III.5.2.1. Procédé de
nébulisation/séchage :
Le procédé de nébulisation/séchage
est un procédé continu en une seule étape qui permet de
transformer une formulation liquide initiale en une forme microparticulaire
sèche. La formulation liquide initiale peut être constituée
:
- Soit d'une solution de matière active et de
matériau enrobant ;
- Soit d'une dispersion de particules solides de matière
active dans une solution ou une émulsion de matériau enrobant
;
- Soit encore d'une émulsion de matière active dans
une solution de matériau enrobant. Ce procédé comprend les
4 étapes séquentielles suivantes :
- Nébulisation de la formulation liquide initiale pour
former un aérosol ;
- Mise en contact de l'aérosol avec un flux d'air,
porté à une température contrôlée ; -
Séchage rapide de l'aérosol pour former des microparticules
solides ;
- Séparation de la poudre de microparticules et de l'air
contenant le solvant vaporisé.
Les microparticules obtenues par
nébulisation-séchage (Le plus souvent des microsphères)
sont d'une taille typiquement comprise entre environ 1 um et 50 um, pour un
séchage à cocourant. Le séchage à contre-courant
permet d'obtenir des microparticules de taille moyenne plus
élevée, comprise entre environ 50 et 200 um.
Le taux d'encapsulation est limité à environ 40 %
(en masse) (Richard et Benoit, 2000).
III.5.2.2. Procédé d'enrobage en lit
fluidisé :
Le procédé d'enrobage en lit fluidisé
s'applique exclusivement à des matières actives
constituées de particules solides (granulés, cristaux). Des
matières actives liquides peuvent néanmoins être
encapsulées après absorption par des supports particulaires
poreux. Le procédé
permet de réaliser un enrobage continu de particules qui
conduit donc à la production de microcapsules. Il comprend une
séquence cyclique en trois temps :
- Fluidisation de la poudre de particules ;
- Pulvérisation du matériau enrobant sur les
particules ;
- Séchage et filmification de l'enrobage.
Les formulations liquides qui sont pulvérisées sur
les particules en mouvement dans le lit fluidisé sont des solutions ou
des dispersions aqueuses ou organiques de polymères.
Quand les gouttelettes de la formulation liquide
pulvérisée rencontrent la surface des particules, la formation du
film d'enrobage s'effectue en plusieurs étapes successives (fig.17) :
- Contact microparticule-gouttelette ;
- Mouillage et étalement de la gouttelette sur la
particule ;
- Séchage par évaporation du solvant et
éventuellement pénétration dans la particule
(Richard et Benoit, 2000).
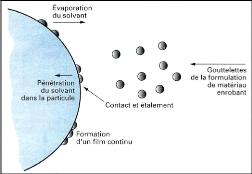
Figure (17) : Etape de formation d'un film
d'enrobage par spraycoating sur
des particules solides (Richard
et Benoit, 2000).
Les paramètres de procédé, qui doivent
être maîtrisés et ajustés pour obtenir un tel
enrobage, sont liés soit au séchage du film, soit à la
pulvérisation de la formulation liquide.
L'épaisseur des films d'enrobage déposés
sur des particules en lit fluidisé est généralement
comprise entre quelques micromètres et 20 um. Le film devant être
suffisamment épais pour masquer les défauts de surface.
Le taux d'encapsulation est généralement
élevé, compris entre 60 et 90 % (en masse) (Richard et
Benoit, 2000).
III.5.2.3. Frocédés de
gélification et congélation de gouttes (Frilling)
:
| 


