A- Gélification de gouttes :
La gélification de gouttes est basée sur la
formation d'une solution, dispersion ou émulsion de matière
active dans une solution aqueuse de polymères capables de former des
gels sous une action extérieure, physique ou chimique. Il s'agit, par
exemple, de l'alginate de sodium,
du chitosan ou de l'agarose. Dans le cas de l'alginate de
sodium, les gouttelettes, formées par extrusion à travers une
buse vibrante, sont réceptionnées dans une phase aqueuse
gélifiante contenant du chlorure de calcium. Elles se transforment
instantanément en des microparticules de gel sphérique (fig.18)
(Richard et Benoit, 2000).
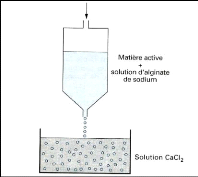
Figure (18) : Schéma de principe du
procédé de gélification
de gouttes
(Richard et Benoit, 2000).
Les microparticules peuvent ensuite être
transférées dans une solution de polylysine, pour former une
membrane rigide semi-perméable par complexation de l'alginate et du
polycation.
Lorsque le chitosane est utilisé, la phase aqueuse de
réception des microgouttelettes est une solution alcaline, qui
insolubilise le chitosane. Dans le cas de l'agar, c'est la variation de
température des gouttelettes de 80 0C à 30
0C qui induit la gélification. La solubilité de la
matière active dans le milieu de réception doit être la
plus faible possible pour minimiser les pertes par solubilisation
(Richard et Benoit, 2000).
B- Congélation de gouttes :
La congélation de gouttes (ou spray-congealing) fait
intervenir un matériau enrobant de type corps gras, glycéride ou
cire à point de fusion relativement bas, compris entre 50 0C
et 120 0C, elle consiste à préparer un fondu de ce
matériau enrobant dans lequel la matière active est
solubilisée ou dispersée soit sous forme particulaire solide,
soit sous forme de microgouttelettes d'émulsion inverse (eau dans
huile). Cette préparation fondue est maintenue à une
température supérieure à la température de fusion
du matériau enrobant et extrudée sous pression à travers
une buse vibrante. Sous l'effet de la vibration, pour une fréquence bien
choisie, le jet fondu est sectionné sous forme de gouttelettes
sphériques de taille uniforme (fig.19).Ces gouttelettes se refroidissent
dans le milieu de chute (air froid, azote ...) et se solidifient pour donner
des microparticules de type microsphère (Richard et Benoit,
2000).
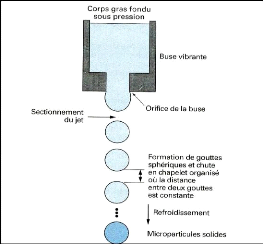
Figure (19) : Congélation de gouttes:
schéma de principe (Richard et Benoit, 2000).
Les microparticules obtenues par ces deux
procédés ont une distribution granulométrique très
étroite, dans une gamme de diamètres accessibles limitée
à des valeurs comprises entre seulement 200 um et 800 um.
Le taux d'encapsulation reste généralement faible
(entre 10 % et 30 % en poids) (Richard et Benoit, 2000).
III.5.3. Procédés chimiques :
III.5.3.1. Polycondensation interfaciale
:
La polycondensation interfaciale est un procédé
qui permet de préparer in situ une membrane polymère à la
surface de gouttelettes d'émulsion, grâce à une
réaction chimique entre deux monomères bien choisis, la
réaction se déroulant à l'interface entre la phase
dispersée et la phase dispersante. La méthode s'applique à
des solutions de matières actives, aussi bien organiques qu'aqueuses, ou
à des matières actives liquides. Le principe de ce
procédé est schématisé sur la figure 20
(Richard et Benoit, 2000).
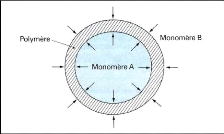
Figure (20) : Mécanisme de la
polycondensation interfaciale (Richard et Benoit,
2000).
La taille des microcapsules obtenues par polycondensation
interfaciale est comprise entre environ 0,5 um et 100 um selon la taille
initiale des gouttelettes d'émulsion (Richard et Benoit,
2000).
III.5.3.2. Autres procédés chimiques
:
Les autres procédés chimiques de
microencapsulation sont des procédés basés sur la
polymérisation radicalaire ou anionique en milieu dispersé. Il
s'agit des procédés de polymérisation en :
- Emulsion ;
- Microsuspension ;
- Dispersion ;
- Miniémulsion ;
- Microémulsion.
Les particules obtenues présentent des tailles
comprises entre quelques dizaines de nanomètres et quelques dizaines de
micromètres, et sont le plus souvent de type matriciel
(nanosphères ou microsphères).
Les taux d'encapsulation sont compris entre quelques pour cent et
50 % (en masse) (Richard et Benoit, 2000).
III.6. Libération contrôlée d'un PA
:
III.6.1. Définition :
Par définition, le rôle d'un système à
libération contrôlée est de délivrer la bonne
quantité d'un PA, au bon endroit et au bon moment.
Lorsqu'on considère les interactions matière
active/milieu extérieur, les microparticules peuvent être
classées en deux catégories: celles qui ne doivent pas
libérer leur contenu telles que les microréacteurs contenant des
enzymes ou des bactéries, et celles qui sont formulées de
façon à libérer la matière active
encapsulée. Dans ce dernier cas, il faut distinguer (fig.21) :
- Systèmes à libération
déclenchée ;
- Systèmes à libération prolongée
(Richard et Benoit, 2000).
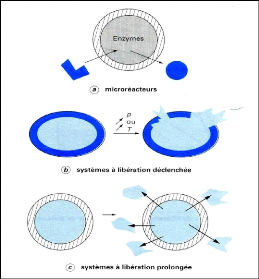
Figure (21) : Microréacteurs et
systèmes à libération déclenchée
et
prolongée (Richard et Benoit, 2000).
III.6.2. Mécanismes de la libération
contrôlée :
Les systèmes à libération
controlée possèdent des exigences particulières au (x)
matériau(x) impliquée (s), qui sont de nature polymérique
sous forme de matériau plein ou d'une membrane (Guery,
2006).
A) Systèmes à libération
déclenchée : sont généralement des
microcapsules formées d'une membrane de faible
perméabilité, qui vont libérer brutalement leur
contenu.
Les mécanismes de la libération connus dans ce cas
sont :
> Mécanismes de libération par
éclatement : sous l'effet d'une pression (mécanique
ou osmotique) ;
> Mécanismes de libération par
fusion : sous l'effet de la température (Guery,
2006).
B) Systèmes à libération
prolongée : sont majoritairement des microsphères
(Guery, 2006) Les mécanismes mis en jeu sont :
> Mécanismes de libération par
dégradation :
La plupart des polymères biodégradables se
dégradent par hydrolyse en composés de taille de plus en plus
faibles, biologiquement éliminables, dans certains
métabolique.
La dégradation peut s'effectuer selon une hydrolyse en
masse,il est uniforme dans toute la matrice polymère ou bien se produire
uniquement sur la surface du polymère.
> Mécanisme de libération par
diffusion uniquement :
La diffusion se produit quand un principe actif traverse le
polymère qui forme le système de libération .La diffusion
peut se produire à l'échelle macroscopique à travers les
pores dans la matrice ou à l'échelle moléculaire par le
passage entre les chaînes de polymères (lois de FICK).
> Mécanismes de libération par
gonflement suivi d'une diffusion :
Parmi les nombreux mécanismes de libération du PA,
nous souhaitons décrire plus particulièrement ce mécanisme
(le cas étudié).
La compréhension des mécanismes de gonflement
des polymères dans l'organisme est importante pour permettre de
concevoir la système particulier de libération
contrôlée et permet d'expliquer les comportements
cinétiques libération. Le PA est dissout ou dispersé au
sein d'une matrice polymèrque capable d'en sortir.
En prémier lieu, le polymère ne subit aucune
modification chimique, il n'est pas dégradé, l'eau diffuse
simplement à l'intérieur du réseau polymère, le
gonfle, ce qui permet aux médicaments piégés a
l'intérieur de se libérer.
Les systèmes de libération
contrôlées par gonflement sont initialement secs et quand ils sont
placés dans le corps, ils absorberont l'eau ou autres fluides du corps
et gonfleront .Ces systéme permettant la diffusion du PA à
travers: le réseau gonflé dans l'environnement externe .La plus
part des matières utilisées dans ces systéme sont les
hydrogels ( absorbant de l'eau ou autres fluides sans être dissoudre).
La capacité du gonflement de polymère se
manifeste quand le gonflement peut être déclenché par un
changement de l'environnement entourant le systéme de la
libération. Dépendant du polymère, le changement
environnement peut impliquer le pH , la température, ou la force
ionique, et le systéme peut se rétrécir ou gonfler sur un
changement de n'importe lequel de ces facteurs environnementaux.
La figure 22 illustre les changements de bases de la structure
de ce systéme sensibles. De nouveau, pour ce type de système, le
dégagement de drogue accompli seulement quand le polymère gonfle
(Xiaoling et Bhaskara, 2006)
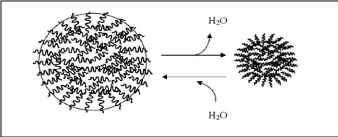
Figure (22) : Processus de gonflement d'un
hydrogel (Igor et Mattiasson, 2008)
À partir d'une microsphère, le
phénomène de diffusion de la molécule active à
travers une matrice sera décrit par une cinétique
obéissant à la loi d'HIGUCHI (Banker et Rhodes,
2002)
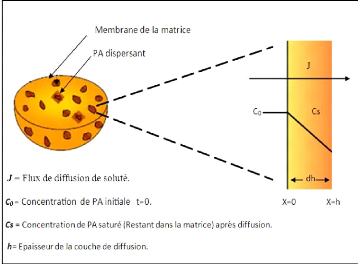
Figure (23) : Représentation
schématique d'une paroi matricielle (Banker et Rhodes,
2002)
= C0 ??h - ??????
d dh

Où :
dm : Variation de la masse de PA liberé par unité
de surface ;
dh : Epaisseur de la couche de diffusion ;
C0 : Concentration de PA initiale t=0 ;
Cs : Concentration de PA saturé (Restant dans la matrice)
après diffusion.
On a aussi à partir de théorie de diffusion :
Dm : Coefficient de diffusion dans la matrice ; t : Temps de
libération ;
À partir les deux équations précedentes et
après lintegration selon h, on trouve la formule suivante :
m = [Cs Dm (2 C0 -- Cs) t]1"2
On a toujours C0 >> Cs, donc
m = [2Cs Dm C0 t]1"2
Pour un systéme matriciel granulair et poreux :
m = [Ds Ca
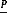
Où :
P : Porosité de la matrice ;
T : Tortuosité ;
Ca : Solubilité de PA dans le milieu de libération
; Ds : Coefficient de diffusion de PA dans le milieu.
On peut réduire cette équation pour obtenir la loi
de HIGUCHI :
m = k t1/2
La loi d'HIGUCHI montre que la quantité
libérée de matière active est directement proportionnelle
à la racine carrée du temps (Banker et Rhodes,
2002).
III.6.3. Param~tres influençant la
libération d'un PA :
Il est à noter que les paramètres
influençant la libération d'un PA encapsulé sont :
- Solubilité du PA dans le milieu de libération et
dans la paroi polymérique ;
- Taux d'encapsulation ;
- Interactions chimiques entre le PA et polymère ;
- - Caractéristiques morphologique de système de
libération (porosité, tortuosité, surface, forme) ;
- - Caractéristiques de polymère tel que poids
moléculaire (des études récentes montrent que les
polymeres de faibles poids moléculaires présentent une
porosité plus élevé que d'autre, donc une
libération plus élevée (Igor et Mattiasson,
2008).
III.6.4. Profils de libération obtenus à
partir de différents types de microparticules : La difusion du
PA selon les modes de la cinétique de libération obeissent aux
trajets de la figure 24 :
À partir des microcapsules, on peut obtenir des
cinétiques de libération d'ordre 0 ou d'ordre 1 (profils A et D),
en fonction de la solubilité dans l'eau de la matière active.
Les cinétiques d'ordre 0 peuvent titre modifiées
dans leur phase initiale: Soit la vitesse de libération est
exagérément marquée (effet de BURST) en raison de la
présence d'un excès de matière active dans la membrane
(profil B), soit un temps de latence qui précède la
libération, temps nécessaire par exemple pour que le principe
actif diffuse à travers la membrane, avant d'atteindre le milieu
extérieur (profil C).
À partir de microsphères, la cinétique
obéissant à la loi d'HIGUCHI (profil E) (Richard et
Benoit, 2000).
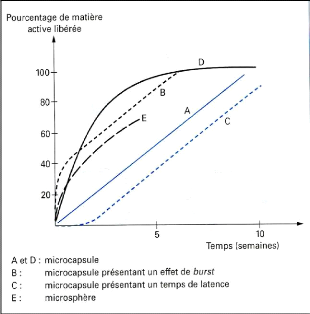
Figure (24) : Profils de libération
obtenus à partir de différents types
de microparticules
(Richard et Benoit, 2000).
Les microparticules à libération prolongée
sont très largement utilisées dans les domaines agroalimentaire
et pharmaceutique (Richard et Benoit, 2000).
III.7. Les polymères :
III.7.1. Définition :
Les polymères sont des matériaux composés
de macromolécules. Celles-ci sont constituées par la
répétition d'unités simples de faible masse
moléculaire, liées entre elles par des liaisons covalentes .Les
molécules qui s'enchaînent pour former le polymère sont
appelées monomères. Lorsqu'un polymère est obtenu à
partir de deux ou de plusieurs monomères différents, il est
appelé copolymère. Dans le cas contraire, on parle alors d
'homopolymère (Dubois, 2004).
III.7.2. Fonctionnalité :
Un monomère doit comporter au moins un groupe
fonctionnel capable de former des liaisons chimiques avec d'autres
molécules de monomère. Le nombre de groupes fonctionnels,
appelé nombre de fonctionnalité, à une influence
très importante sur la structure et les propriétés du
polymère. Un nombre de fonctionnalité unitaire entraîne la
synthèse de polymères linéaires; un nombre de
fonctionnalité supérieur permet la formation de polymères
réticulés (fig.25) (Dubois, 2004).
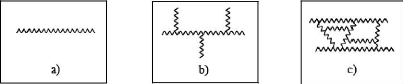
Figure (25) : Représentation
schématique de polymères
linéaires (a), ramifiés
(b) et réticulés (c) (Dubois, 2004).
III.7.3. Classification des polymères
:
Les polymères peuvent être classés selon
différents critères qui sont :
> Selon leur origine :
- Polymères naturels: sont issus des règnes
végétal ou animal, on peut cependant mentionner, la famille des
polysaccharides (cellulose, amidon), celle des protéines (laine,
soie...) ;
- Polymères artificiels : élaborés
chimiquement à partir d'un monomère naturel ;
- Polymères synthétiques : sont obtenus par
polymérisation de molécules monomères (les
monomères utilisés n'existent pas dans la nature).
> Selon la fonction géométrique
:
- Mono-dimensionnelle ;
- Bi-dimensionnelle ;
- Tridimensionnelle.
> Selon les propriétés
physico-chimiques :
- Polymères thermoplastiques (ou thermoplastes) : sont
constitués de macromolécules de taille limitée
linéaires ou ramifiées. Ils peuvent passer de l'état
rigide à l'état malléable par une faible
élévation de température. Ce processus est en
général réversible, ce qui confère à ces
polymères une certaine facilité de mise en oeuvre et de
recyclage. A ce jour, sont regroupés dans cette famille les
polymères dont la cohésion latérale est assurée par
des liaisons faibles (liaisons de type VAN DER WAALS, liaisons
hydrogènes) ;
- Elastomères, matériaux obtenus à partir
de polymères linéaires ayant des liaisons secondaires très
faibles. Ces matériaux sont ainsi considérés comme des
liquides très visqueux. L'introduction d'un certain nombre de liaisons
pontales entre les chaînes confère aux élastomères
une structure tridimensionnelle. Leur caractéristique principale est
leur grand déformabilité qui peut dépasser les 1000%. Ceci
est principalement dû à leur faible densité de
réticulation. Par ailleurs, le pontage rend les
élastomères difficilement recyclables ;
- Polymères thermodurcissables, qui sont des
polymères fortement réticulés. En effet, leur taux de
réticulation est de 10 à 100 fois plus élevé que
dans les élastomères. Ils forment un réseau
tridimensionnel et on peut considérer qu'ils ne sont constitués
que par une seule macromolécule d'une taille infiniment grande à
l'échelle atomique. Les fortes liaisons qui existent entre les
chaînes confèrent à ces polymères une
résistance mécanique et thermique nettement supérieure
à celle des thermoplastes. Les polymères thermodurcissables sont
insolubles, infusibles et non recyclables.
> Selon leur structure :
- Polymères amorphes, caractérisés par une
absence d'ordre des chaînes macromoléculaires. Celles-ci
s'enlacent les unes les autres, se replient sur elles mêmes. Ces
polymères sont habituellement imagés à un
plat de spaghetti cuit ;
- Polymères semi-cristallins,
caractérisés par la présence d'arrangements
réguliers des chaînes macromoléculaires reliés dans
une matrice amorphe, le taux de cristallinité caractérise
l'importance de structure cristalline (Dubois, 2004).
III.7.4. Polymères utilisés dans la
microencapsulation :
Dans la microencapsulation, variété de
polymères sont utilisés, on distingue :
Dans le cas de procédés physico-chimiques et
mécaniques, la formulation des microparticules met en oeuvre des
matériaux enrobant préformés, d'origine très
variées, qui sont choisis parmi des grandes classes.
(voir tableau 05 annexe I).
Dans le cas de procédés chimiques les
monomères utilisés sont habituellement:
- Monomères acryliques et méthacryliques de type
ester (acrylate de butyle, méthacrylate de méthyle ...) ou
porteurs de groupements fonctionnels tels que des acides carboxyliques (acide
acrylique ...), ou des fonctions hydroxyle (méthacrylate
d'hydroxyéthyle) ;
- Monomères vinyliques (acétate de vinyle ...) et
le styrène ;
- Monomères de type cyanoacrylate d'alkyle (cyanoacrylate
d'isohexyle).
Les deux premiers types de monomères réagissent
par un mécanisme radicalaire, alors que le troisième type
polymérise par voie ionique (voir tableau 06 annexe I)
(Richard et Benoit, 2000).
III.7.5. Acide alginique :
Acide de formule générale
(C6H10O7) n extrait des parois cellulaires
des Algues brunes. L'acide alginique est un biopolymère constitué
d'une succession de blocs formés de deux unités
monosaccharidiques : l'acide D-mannuronique (Ma) et son epimère en C5,
l'acide L-guluronique (Gu), liés en 1et 4 par des liaisons
glycosidiques, pour former une chaîne polymérique linéaire.
La proportion et la distribution de ces monomères déterminent en
grande patrie les propriétés de l'alginate. Les sels de l'acide
alginique sont nommés alginates, on distingue: les alginates de sodium,
de potassium et d'autres métaux alcalins sont parfaitement solubles dans
l'eau en donnant des solutions à haute viscosité, tandis que
l'acide alginique pur et son sel de calcium sont pratiquement insolubles dans
l'eau (Anonyme 10).
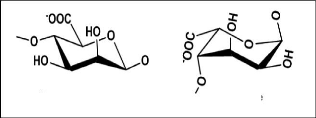
D-mannuronate L-guluronate
Figure (26) : Unités
monosaccharidiques constituant l'alginate (Onesippe,
2005).
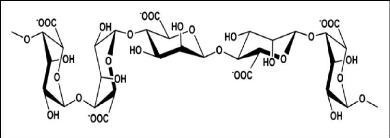
Figure (27) : Structure chimique de
l'alginate (Onesippe, 2005).
L'alginate a la
propriété de réticulation et ce dans les régions
d'acide guluronique quipeuvent être liées à une
région similaire dans une autre molécule d'alginate via le
Ca++ ou un
autre cation multivalent.
Du fait de leur absence de toxicité et de leur
capacité à former des gels, les alginates sont utilisés
dans de nombreux domaines (Anonyme 10).
| 


