Chapitre 5
DYNAMIQUE MOLECULAIRE DU SUCRE CONFINE DANS UN GEL DE
SILICE AQUEUX
5.1. Dynamique du D-glucose confiné dans des gels de
silice 115
5.2. Dynamique du tréhalose confiné dans des gels
de silice 122
5.3. Conclusion générale du chapitre 5 128
CHAPITRE 5
DYNAMIQUE MOLECULAIRE DU SUCRE CONFINE DANS UN GEL DE SILICE
AQUEUX
D'après le chapitre précédent, il
émerge que les sucres présentent une forte aptitude à
conserver les édifices dans leur intégrité structurale.
Cette conclusion confirme donc les hypothèses avancées pour
expliquer la résistance des organismes anhydrobiotiques. Si cette
étude structurale nous apporte une confirmation supplémentaire du
rôle crucial des sucres, il reste néanmoins qu'elle ne fournit pas
à elle seule quelles en peuvent être les causes ? Parmi les
hypothèses évoquées pour de si grandes pertes en eau, la
substitution de l'eau d'hydratation et la vitrification sont les deux
phénomènes les plus probables. (Cf. Chapitre 1) Or ces deux
hypothèses sont basées sur des questions d'interaction eau-
soluté principalement. Ainsi, pour comprendre les origines mêmes
de cette protection, il est absolument nécessaire d'étudier les
aspects dynamiques des molécules de sucre, qui peuvent donner un
aperçu des interactions au sein de ces solutions. Dans ce chapitre, nous
allons donc étudier la dynamique des molécules de D-glucose d'une
part, puis celle des molécules d' tréhalose d'autre part,
confinées dans ces mêmes gels de silice. Nous pourrons donc
regarder les effets de la taille de l'environnement sur leurs dynamiques
respectives.
5.1. DYNAMIQUE DU D-GLUCOSE DANS LES GELS DE SILIC
5.1.1. Conditions expérimentales
Les mesures de dynamique moléculaire du D-glucose
confiné, par diffusion quasi-élastique des neutrons, ont
été réalisées au National Center for Neutron
Research (NCNR) sur les spectromètres DCS85 et
HFBS.86 La gélification des sols s'est faite directement dans
des porte-échantillons cylindriques d'espace annulaire 0,4 mm. Une fois
scellés, ils ont été placés dans un cryostat dans
lequel la température est régulée à #177; 1 K.
Les trois échantillons A1, A2 et A3 ont
été mesurés sur le DCS à 300 K, avec une longueur
d'onde incidente de 6 Å (0,25 < Q < 1,93 Å-1), et
pour une résolution instrumentale de 57p,eV. Pour les mesures
effectuées sur le HFBS, les paramètres expérimentaux
étaient les suivants : T = 300 K, 2%, = 6,27 Å, 0,36 < Q <
1,52 Å-1 avec une résolution de #177; 1,2 geV.
5.1.2. Traitement des données
Les spectres de chaque échantillon ont
été normalisés au moniteur, corrigés de la cellule
vide, normalisés au vanadium, puis regroupés afin
d'améliorer la statistique. Cette partie du traitement est en tout point
identique à celle décrite précédemment (Cf.
Chapitre 2 : p. 40).
Afin d'extraire la dynamique des molécules de
D-glucose, nous avons soustrait le gel sans sucre A1 des gels contenant du
sucre (A2 et A3), les spectres résultants s'appelleront respectivement
A2-A1 et A3-A1. Afin de prendre en compte les différents facteurs
d'atténuation du gel pur (A1) et des gels contenant du sucre (A2 et A3),
la diffusion de A1 a été multipliée par le facteur
d'atténuation du D- glucose avant la soustraction. Le coefficient
d'atténuation d'une espèce se calcule à partir du nombre
d'atomes i par unité de volume ñi, de la section efficace de
diffusion totale i, de la section efficace
S
i
d'absorption, et enfin du chemin optique x :
A
i i
A exp ( )
ñ x
espèce i S A
i?espèce
Si l'on suppose que la densité partielle du gel n'est
pas affectée par la présence du sucre, alors le
coefficient
d'atténuation d'un gel contenant du sucre est le produit des
coefficients d'atténuations du
gel et du sucre : A gel A gel × A glucose .
glucose
A titre d'exemple, la soustraction pour le gel A2 s'est
effectuée de la manière suivante:
A2 - A1A2AgelglucoseCVA × glucoseA1 × AgelCV
où Agel+glucose est le coefficient d'atténuation du
gel A2, Aglucose celui du D-glucose, et CV le signal de la cellule vide.
La validité de la procédure repose bien
évidemment sur l'hypothèse que la présence du sucre
n'affecte pas la dynamique du gel hôte. Cette hypothèse est
supportée par le fait que le gel est deutéré et qu'il
contribue donc relativement peu à la diffusion totale. (Tableau 25)

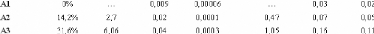
Tableau 25: Contributions relatives de la diffusion
cohérente et incohérente émanant du D-glucose, de l'eau
lourde et du gel.
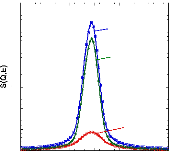
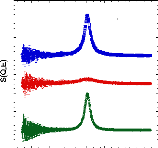
Les fonctions de diffusion des échantillons A1 et A3,
et de la soustraction A3-A1, sont présentées sur la figure 51(a)
pour le DCS pour Q = 0,7Å-1 et sur la figure 51(b) pour le
HFBS pour Q = 0,36Å-1. Celles-ci montrent de manière
claire que la contribution solvant/matrice est faible en comparaison de celle
du D-glucose.
35
30
(a)
Q = 0.744
T = 300 K
A3
25
A3-Al
20
1 5
10
5
0
Al
-0.3 -0.2 -0.1 0 0.1 0.2 0.3
E (meV)
-40 -30 -20 -10 0 10 20 30 40
(3)
T = 300 K Q = 0,3644
A3-Al
A3
Al
E (peV)
Figure 51: Fonctions de diffusion pour les échantillons A1
(rouge), A3 (bleu) et A3-A1 (vert) tirées des mesures
réalisées sur le DCS (a) et sur le HFBS (b) à 300 K.
| 


