Partie II. Caractérisation du principe actif
(Ibuprofène pur)
II.1. Analyse thermique
II.1.1. Etude TG/DTG
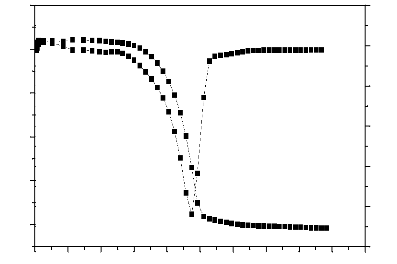
La figure 64 montre les courbes TG/DTG obtenues à 0,5
°C/min sous atmosphère d'azote pour l'ibuprofène pur. Les
courbes ATG-ATD de l'ibuprofène montrent une stabilité thermique
jusqu'à 125 °C. La décomposition thermique s'effectue entre
125 et 264 °C avec une perte de masse totale correspondante au pic
endothermique à 237,2 °C, ces résultats sont en accord avec
la littérature (G. Bannach, 2010).
dm/dt (%/min)
-10
-15
-20
-5
0
5
0
0 50 100 150 200 250 300 350 400 450 500
40
20
60
80
120
100
m (%)
TG
DTG
Température (°C)
Figure 64. Courbe de TG/DTG obtenu à 10
°C/min sous atmosphère d'azote pour l'ibuprofène pur.
II.1.2. Analyse DSC
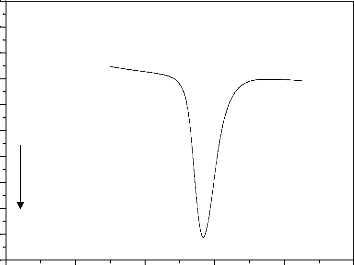
La courbe DSC de l'ibuprofène pur est donnée
dans la figure 65. D'après cette dernière, l'ibuprofène
montre un pic endothermique correspondant à son processus de fusion
à 76,7 °C avec un enthalpie de fusion ÄHf de 61,29 J/g, ce
résultat est en accord avec celui trouvé par Juliana Bidone et
al. (J. Bidone, 2009).
Endotherme
Tf = 76,69 °C
0,2
0,0
-0,2
Flux de chaleur (mW.mg-1)
-0,4
-0,6
-0,8
-1,0
-1,2
-1,4
-1,6
-1,8
20 40 60 80 100 120
Température (°C)
Figure 65. Courbe DSC de l'ibuprofène
pur.
II.2. Analyse structural
II.2.1. Spectre IR-TF de l'ibuprofène
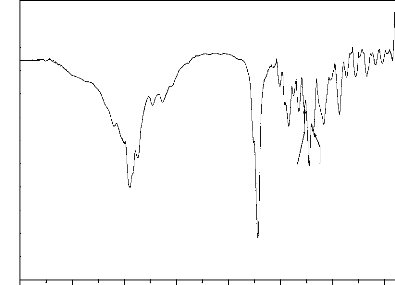
La figure 66 montre le spectre Infrarouge à
Transformé de Fourier (IR-TF) de l'ibuprofène pur. La comparaison
avec les spectres de l'ibuprofène trouvés dans la
litérature (J. Namur, 2009 ; G. Bannach, 2010), nous a
permet d'indexer notre spectre, et le tableau 18 suivant résume les pics
caractéristiques de l'ibuprofène pur ainsi que les types de
vibration des liaisons correspondates.
Tableau 18. Les bandes d'absorption infrarouge
caractéristiques de l'ibuprofène pur.
|
Nombre d'onde í (cm-1)
|
Liaison et type de vibration
|
|
3090
|
Vibration d'élongation de C-H aromatique
|
|
2955
|
Vibration d'élongation antisymétrique de CH3
|
|
1720
|
Vibration d'élongation de C=O (COOH)
|
|
1509
|
Vibration d'élongation de C-C cyclique
|
|
1420
|
Vibration élongation/déformation
antisymétrique de C-C-O-H
|
|
1269
|
Vibration d'élongation de C-O (COOH) et vibration de
|
|
1230
|
déformation de O-H
|
|
1184
|
|
|
935
|
Vibration de déformation hors du plan de O-H
(dimère acide)
|
3090
935
1420
2955
1269
1230
Transmittance (%)
1184
1720
4000 3500 3000 2500 2000 1500 1000 500
Nombre d'onde (cm-1)
Figure 66. Spectre IRTF de l'ibuprofène
pur.
II.2.2. Spectre DRX de l'ibuprofène
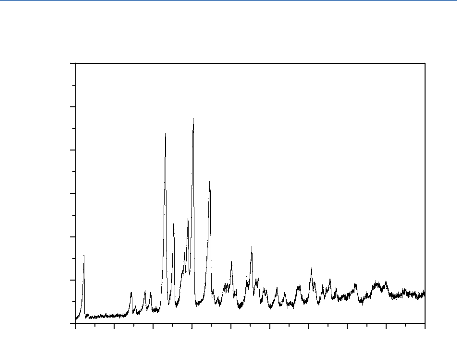
La diffraction des rayons X de l'échantillon
ibuprofène pur est donnée dans la figure 67. Le spectre DRX de
l'ibuprofène a révéle des reflexions de fortes
intensités et elles correspond aux distances
interétéculaires suivantes : 14,4, 7,2, 5,3, 4,4 et 4,0 avec des
pics caractéristiques à 6,1°, 12,3°, 16,6°,
20,2°, et 22,4°, respectivement, et ces résultats sont
comparables à ceux trouvés dans la litérature (J.
Bidone, 2009 ; N. V. Phadnis, 1997 ; A. FernándezCarballido, 2004 ; C.
Acquah, 2009).
3000
2500
2000
1500
1000
500
0
5 10 15 20 25 30 35 40 45 50
2 Thêta (°)
Intensite
16,632°
20,221°
22,390°
6,139°
12,257°
Figure 67. Spectre DRX de l'ibuproféne
pur.
| 


