IV. Cycle du développement des
Plasmodiums
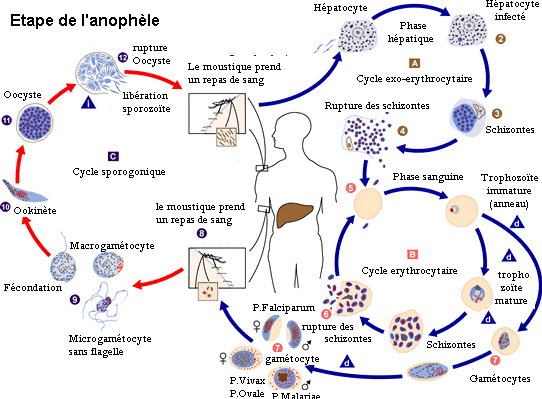
En fonction de ses deux hôtes, le vertébré
(homme) et l'invertébré (moustique) on divisera le cycle
évolutif du Plasmodium en deux grandes parties à savoir la
schizogonie et la sporogonie.
1. Cycle évolutif chez l'homme (schizogonie)
Suivant les tissus qu'ils occupent majoritairement chez
l'homme ce cycle se divise en cycle pré-érythrocytaire
(hépatique ou symptomatique) et cycle érythrocytaire, ce dernier
conduit à la fièvre suite à l'éclatement des
globules rouges. (3)
Cycle
pré-érythrocytaire (hépatique ou
asymptomatique)
Les plasmodiums sous forme de sporozoïtes sont
inoculés lors de la piqûre d'un anophèle femelle
infesté et gagnent les hépatocytes. En se multipliant, ils se
transforment en schizonte extraérythrocytaire ou intra-hépatique
(corps bleu). L'éclatement des corps bleu libère des
mérozoïtes. (3)
Cycle érythrocytaire (symptomatique)
Les mérozoïtes gagnent le sang
périphérique et parasitent les globules rouges en devenant, au
fur et à mesure de leur croissance, trophozoïtes, schizontes
sanguins puis corps en rosace.
Les corps en rosace éclatent libèrent des
mérozoïtes. L'apparition des éléments à
potentiel sexué ou gamétocytes est plus tardive. (3)
2. Cycle évolutif chez le moustique (sporogonie)
Les gamétocytes aspirés avec le sang par le
moustique lors de son repas, gagnent son estomac pour se transformer en
gamète. Après fécondation les gamètes femelles
deviennent des ookinètes libres, puis oocystes fixes.
L'éclatement des oocystes libère des sporozoïtes qui gagnent
les glandes salivaires de l'anophèle à partir desquelles ils
peuvent être retransmis à un autre hôte
vertébré (homme).
Il est à noter que P. ovale et P. vivax avant de passer
à la forme schizonte hépatique, leur mérozoite peut
passer par la forme hypnozoïte qui est susceptible de se réveiller
après plusieurs mois ou plusieurs années. (3)
D. Réactions immunitaires de l'hôte humain et
mécanismes de survie du parasite
1. Réactions immunitaires
Immunité non adoptive (naturel) :
La compatibilité hôte-parasite ne dépend
nullement des facteurs sériques, mais de la présence des
récepteurs spécifiques présents sur les membranes des
parasites et des érythrocytes. Il peut être observé dans
certains cas une résistance au paludisme. (2)
Tous les plasmodiums en général ne
résistent pas chez les individus ayant un déficit en
6-phosphoglucose réductase (6-GPDH).Le P. vivax ne subsiste pas chez les
individus non porteurs du gène Duffy qui assure la synthèse des
récepteurs nécessaires à la pénétration de
sa forme merozoïte dans le globule rouge. (2)
Les facteurs intra-érytrocytaires seraient responsables
du ralentissement de l'acquisition de l'immunité des blancs par rapport
aux noirs dans la malaria à P. falciparum. L'hémoglobine S inhibe
le développement de la schizogonie du P. falciparum. C'est pourquoi on
n'observe pas d'accès pernicieux chez les sujets drépanocytaires
hétérozygotes. (2)
Les anomalies du cytosquelette telles que l'ovalocytose ou
ellipocytose, s'opposent à l'induction de l'endocytose du plasmodium
dans l'érythrocyte. (2)
Immunité acquise (adoptive)
La réponse immunitaire exprimée par la
production de différentes classes d'immunoglobulines semble
principalement être dirigée contre les formes
érythrocytaires asexuées du plasmodium. Les anticorps produits
sont de faible affinité et la mémoire immunologique induite est
de très courte durée (1 à 2 ans pour le P. falciparum).
(2)
Dans les six premiers mois de la vie, l'enfant né d'une
mère immune est relativement protégé contre les
accès palustres grâce à l'immunité passive, avec les
immunoglobulines, transmise par la mère via le placenta. Ayant par la
suite perdu cette immunité passive, il devient, avant d'avoir
réussi à constituer ses progrès en défenses
immunitaires, avant l'âge de cinq ans, un sujet particulièrement
vulnérable. C'est cette strate de la population en zone endémique
qui paie le plus lourd tribut au paludisme. (2)
L'état de grossesse, surtout le premier trimestre et le
second dans une certaine mesure, induit une immuno suppression dite
physiologique qui amplifie malencontreusement la pathogénicité de
P. falciparum pour cette strate de la population, et compromet ainsi la
prémunition passive au nouveau-né. (2)
2. Mécanismes de survie parasitaire
Les plasmodiums présentent au cours de leur cycle
évolutif différents motifs antigéniques superficiels qui
sensibilisent de façon variée le système immunitaire de
l'hôte : sporozoïtes, schizontes sanguins, schizontes
hépatiques et gamétocytes. (2)
Chacun de ces antigènes induit une réponse
immunologique spécifique de faible amplitude qui ne suffit nullement
à conférer au sujet infecté une
immunité vraiment efficace et de longue durée, d'où
il y aura une ré-infection habituelle des sujets déjà
immuns. Et ceci s'observe dans les zones endémiques où circulent
plusieurs variants antigéniques différents d'un isolat à
l'autre et contre les quels l'hôte n'est pas nécessairement
immunisé. (2)
La recombinaison des gènes par la reproduction
sexuée dans l'estomac du moustique, participe au brassage et au
renouvellement de cette capacité de variation antigénique qui
paralyse la machinerie immunitaire de l'hôte. Toutes les 48 heures le P.
falciparum peut modifier environ 20% de la structure primaire de ses
protéines de surface, on dit qu'il joue au dé avec notre
système immunitaire. (2)
Certaines souches de P. falciparum acquièrent la
capacité d'expurger de leur cytoplasme certaines substances
antipaludiques, notamment la chloroquine, 40 à 50 fois plus vite que ne
ferait une souche normale, ce qui explique leur résistance
vis-à-vis de ces produits. (2)
| 

