2.6.2.2. Protocole d'amplification par PCR (Scott et al.,
1993)
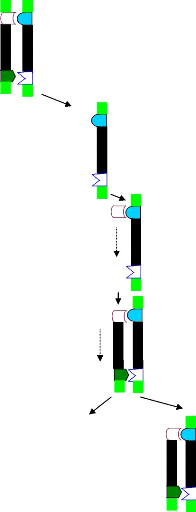
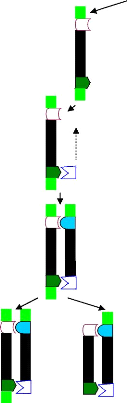
Principe (Fig. 8)
La polymérisation en chaîne est basée sur
le principe de la réplication de l'ADN double brin lors de la mitose
(Clavel, 1993). Cette réaction se fait sur plusieurs cycles comprenant
chacun 3 étapes:
- la dénaturation, phase au cours de
laquelle l'ADN double brin est dénaturé en simple brin par
l'augmentation de la température entre 90°C et 97°C (De
Bruijn, 1988 ; Innis et Gelfand, 1990). En fonction de la longueur et de la
composition en bases de la séquence d'ADN cible, cette phase de
dénaturation dure de 15 à 30 secondes. En général,
la dénaturation de tout le génome dure 5 minutes à une
température de 94°C;

ADN génomique
Séquence d,ADN à amplifier
3,
5,
3,
5,
5,
3,
5,
3,
5,
3,
5,
3,
5,
Dénaturation ou
séparation des brins d,ADN
Hybridation
des amorces
3,
ADN néoformé

Polymérisation ou
extension des amorces
par l,ADN
polymérase
Dénaturation Hybridation puis polymérisation
|
Séquences d,ADN complémentaires
Amorces
|
5,
|
|
Sens de l,extension
|
|
|
3,
|
Figure 8 : Schéma du principe de la PCR
(Polymerase Chain Reaction)
A chaque cycle 2n brins d,ADN
néoformés sont produits (n = nombre de cycles)

- l'hybridation, phase de refroidissement au
cours de laquelle les amorces s'apparient (ou s'hybrident) à leur
séquence complémentaire sur l'ADN cible. La température
d'hybridation varie entre 50°C et 72°C. Elle dépend de la
séquence et du nombre de nucléotides des amorces;
- l'élongation, au cours de laquelle
chaque amorce fixée sur l'un des brins va s'étendre à
partir de son côté 3' par juxtaposition de nucléotides
(dNTPs) par l'ADN polymérase. L'élongation des amorces se fait en
sens opposé en intercalant la séquence à amplifier. Elle
dure de 30 secondes à 2 minutes et se déroule à une
température de 72°C.
Ces 3 étapes sont en général
répétées 20 à 35 fois (Saïki et al.,
1985; Tosi et Acuto, 1992) selon les quantités d'ADN de
départ.
Le milieu réactionnel a été
préparé comme l'indique le tableau 1. Cette solution a
été distribuée dans des microtubes à paroi fine de
0,2ml (25ul par microtube), contenant au préalable deux pattes de
moustiques. Les microtubes sont ensuite fermés et placés dans le
thermocycleur pour l'amplification de l'ADN. La figure 9 représente les
cycles des températures de cette amplification.
2.6.2.3. Protocole de la digestion enzymatique (Favia et
al., 1997)
Le milieu réactionnel est préparé comme
l'indique le tableau 2. Cette solution a été distribuée
dans des microtubes à paroi fine de 0,2ml (15ul par micro tube). Dans
chaque micro tube, nous avons ajouté 10ul de solution d'ADN
amplifié. Les microtubes sont fermés et placés dans
l'étuve (37°C) pendant 3 heures au minimum ou toute la nuit. Les
fragments d'ADN amplifiés sont digérés avec une enzyme de
restriction (Favia et al., 1997); cette enzyme (Hhal : Haemophilus
haemoliticus) coupe le fragment au niveau des sites de restriction de la
manière suivante.
5'&&&&&&.GCGC.&&&3'
3'&&&&&.
CGCG&&&.5'
Ainsi, la digestion de deux ADN différents pour un
locus donné produit des fragments de longueurs différents dont la
migration sur un gel d'agarose à 2% permet de déterminer les
formes moléculaires M et S chez An. gambiae s.s.


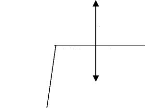
35 cycles
72°
72°
5'
56°
20''
94° 94°
3' 30''

30''

Dénaturation Hybridation Elongation
Figure 9 : Cycle des températures d'une
PCR pour l'identification des espèces et des formes moléculaires
d'Anopheles gambiae s.s (Fanello et al., 2002)
Tableau 2 : Composition du milieu
réactionnel d'une PCR pour l'identification des espèces du
complexe An. gambiae (Scott et al., 1993)
|
Réactif
|
Concentration initiale
|
Concentration finale
|
Volume (ul) par tube
|
|
ddH2O
|
|
|
19,45
|
|
Tampon (+MgCl2)
|
10X
|
1X
|
2,50
|
|
dNTPs
|
5mM
|
0,2mM
|
1,00
|
|
UN*
|
10uM
|
5pmoles
|
0,50
|
|
AR*
|
10uM
|
5pmoles
|
0,50
|
|
GA*
|
10uM
|
5pmoles
|
0,50
|
|
ML*
|
10uM
|
5pmoles
|
0,50
|
|
Taq DNA polymérase ADN
|
5UI/ul pattes
|
0,25UI
|
0,05
|
|
Total
|
|
|
25,00
|
dNTPs : Dinucléotide triphosphates ; UN : Amorce
universelle ; AR : Amorce arabiensis ; GA : Amorce gambiae ;
ML: Amorce melas ; * : Séquence et taille des bandes
présentées en annexe 2 ; ddH2O : Eau bi-distillée ; UI :
Unité internationale ; X : concentration de la solution tampon.

Tableau 3 : Composition du milieu
réactionnel pour la digestion enzymatique de l'ADN d'An. gambiae
s.s (Favia et al., 1997).
|
Réactif
|
Concentration initiale
|
Concentration finale
|
Volume (ul) par tube
|
|
ddH2O
|
|
|
12,00
|
|
Tampon
|
10X
|
1X
|
2,50
|
|
BSA
|
10mg/ml
|
0,1mg/ml
|
0,25
|
|
Enzyme
|
10UI/ul
|
0,1UI/ul
|
0,25
|
|
ADN
|
ADN amplifié
|
|
10,00
|
|
Total
|
|
|
25,00
|
X : Concentration de la solution tampon; BSA: Bovine serum
albumin; ddH2O : Eau bidistillée ; UI : Unité internationale.
Témoins
+
Sens de migration
M M M M M M M M M MM M MT N A M
S
-
Puits de dépôt
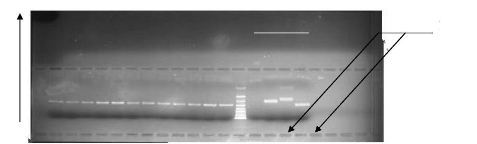
Figure 10: Photographie d'un gel montrant
l'identification de An. gambiae s.s de forme moléculaire M.
MT : marqueur de taille (100 pb) ; M : forme moléculaire M
(367 pb) ; S : forme moléculaire
M S
S (257 pb) ; A : An. arabiensis (292 pb) ; N :
négatif ; pb : paire de base.

| 


