8- Origine des éléments chimiques :
Les eaux souterraines qui circulent dans la nappe alluviale de
Tébessa proviennent des formations carbonatées de l'Eocène
et du Maestrichtien qui bordent la plaine et aussi de l'infiltration. Ensuite,
elles s'écoulent dans un matériel très
hétérogène (des alluvions, des sables, des graviers, des
dépôts évaporitiques...etc.). Le parcours
d'écoulement et les couches traversées influent sur l'acquisition
des éléments chimiques. En se basant sur les mesures et les
analyses chimiques trouvés, on va essayer de déterminer l'origine
probable de tous les ions.
8-1- Les éléments Ca2+ - HCO3 - - SO4 2-
:
Le calcium tire son origine des carbonates et du gypse, la
détermination de l'origine de chaque concentration en Ca2+
est nécessaire pour connaître les mécanismes du chimisme de
la nappe.
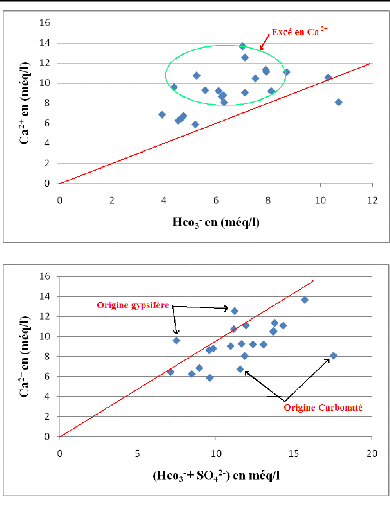
Figure 44A: Détermination de l'origine du
calcium.
Figure 44B: Détermination de l'origine du
calcium.
Nous avons établi un graphe où nous avons
représenté le calcium en fonction des bicarbonates et des
sulfates (figure 44B).
8-2- Les éléments Na+ - Cl- :
Dans les eaux naturelles, la présence des deux
éléments Na+ et Cl- est attribuée à la
dissolution
de la halite que l'on rencontre dans les formations triasiques.
Cependant, les chlorures comme le sodium peuvent avoir d'autres origines
(naturelles ou anthropiques).
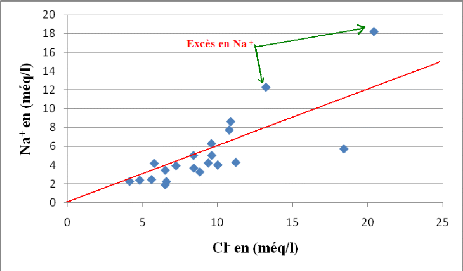
Figure 45A : Détermination de l'origine du
sodium.
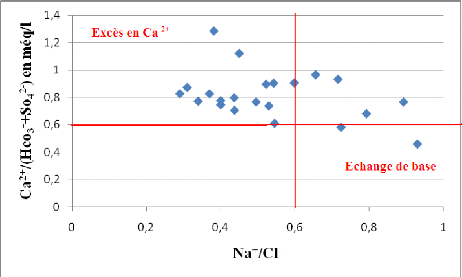
Figure 45B : Détermination de l'origine du
sodium.
La représentation graphique de l'évolution du
Na+ en fonction de Cl (Figure 45A) a montré un excès
des teneurs en Na+, qui s'explique par l'existence d'une autre
origine pour les ions sodiques (autre que l'halite).
L'augmentation des teneurs en Na+ qui a
accompagné les faibles teneurs en Cl est due au phénomène
d'échange de base (Figure 45B), car les argiles du substratum peuvent
libérer des ions Na+ après avoir fixé le
Ca2+.
Les fortes teneurs en Na+ qui ont accompagné
celles élevées du Cl , sont attribuées à la
dissolution de l'halite contenue dans les marnes et aux évaporites du
Trias de Djebel Djebissa. Ce diagramme a confirmé un excès de
Ca2+ par rapport à Na+.
2-:
8-3- Les éléments HCO3 -, Cl- et SO4
Après avoir fait le point sur les origines des cations,
on a essayé de représenter l'évolution des
anions en fonction de la conductivité.
L'interprétation de la Figure 46A montre que la conductivité
électrique n'évolue pas avec les bicarbonates, alors que les
chlorures et les sulfates croissent avec la salinité. Cette
dernière est donc due aux éléments salifères.
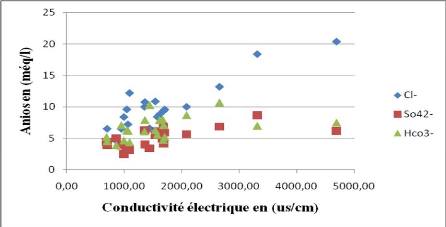
Figure 46A : Evolution des anions en fonction de la
conductivité électrique.
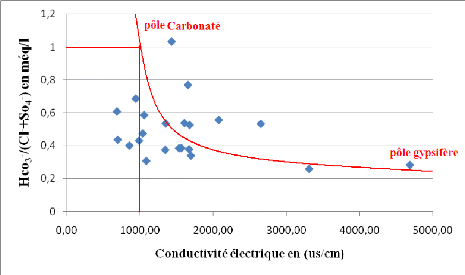
Figure 46B : Evolution des anions en fonction de la
conductivité électrique.
La réalisation d'un diagramme (HCO3-/
Cl- et SO42-) - Conductivité
électrique a montré la présence de deux pôles : le
premier est carbonaté et se caractérise par une dominance des
ions HCO3 -.
| 

