8-4- Les éléments Cl- - SO4 - :
Ces deux ions sont issus de deux formations différentes,
le SO42- provient du gypse et le Cl-
provient de la dissolution de l'halite et probablement d'une
pollution anthropique. On a associé l'évolution de ces ions
à la conductivité électrique pour mettre en relief la
façon selon laquelle ils évoluent et déterminer lequel
entre eux est à l'origine de la salinité des eaux de la nappe.
L'interprétation du graphe (Figure 47) a
révélé que la majorité des points d'eau
présente un rapport (Cl-/SO42-) supérieur
à 1, indiquant ainsi la dominance des ions Cl- par rapport
à SO42-, ce
qui confirme la dominance du faciès chloruré
calcique et sodique. Quelques points d'eau
présentent des valeurs du
rapport (Cl-/SO42-) inférieures à
l'indiquant une origine gypsifère
(Figure 47).
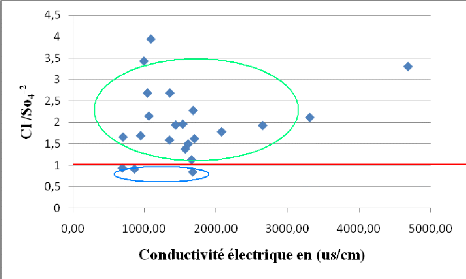
Figure 47 : Evolution des chlorures et des sulfates en
fonction de la
conductivité.
8-5- Etude de l'acquisition de la minéralisation
:
Les eaux météoriques commencent à
acquérir leur minéralisation dès les premières
pluies, où elles se chargent en une faible concentration
d'éléments chimiques. Une fois interceptées par le sol,
une partie des eaux de précipitation ruisselle à la surface et
l'autre s'infiltre dans le sous sol pour atteindre la nappe. Les eaux de
ruissellement vont s'écouler vers les oueds où elles subiront une
évaporation sous l'effet de la température, ce qui produit une
précipitation des éléments chimiques sous forme de
minéraux.
Les eaux qui s'infiltrent dans les formations géologiques
:
- calcaires de bordures, seront chargées en ions
Ca2+, HCO3 -, par la dissolution. Les puits qui se trouvent à
proximité des bordures attestent de cette minéralisation et se
caractérisent par un faciès bicarbonaté calcique.
- riches en gypses et en sels, ce qui leur permet
d'acquérir des concentrations importantes en Na+,
Cl-, Ca2+, SO42-.
-L'irrigation par des eaux salées provoque la salinisation
des sols et augmente ainsi la minéralisation.
Tableau 13 : Les éléments chimiques
rencontrés et leurs sources naturelles.
|
Elément
|
Concentrations
habituellement
rencontrées (mg/L) hors pollution
|
Sources potentielles
|
|
Calcium (Ca2+)
|
Centaines de mg/L
|
Le calcium (Ca2+) et le magnésium
(Mg2+) sont présents dans les roches cristallines et les
roches sédimentaires. Ils sont très solubles et sont donc
largement représentés dans la plupart des eaux.
|
|
Magnésium (Mg2+)
|
Dizaines de mg/L
|
|
Sodium (Na+)
|
Dizaines de mg/L
|
Le cation sodium (Na+) est très abondant sur la
terre. On le retrouve dans les roches cristallines et les roches
sédimentaires (sables, argiles, évaporites). La roche Halite
(évaporite NaCl) est le sel de cuisine. Il est très soluble dans
l'eau
|
|
Potassium (K+)
|
Inférieur à 10 mg/L
(hormis pour les eaux ayant traversé des formations
évaporitiques)
|
Le potassium (K+) est assez abondants sur terre, mais
peut fréquent dans les eaux. En effet, il est facilement adsorbé
et recombiné dans les sols (sur les argiles notamment). Les sources
principales de potassium sont les roches cristallines.
|
|
Bicarbonates (HCO3-)
|
Centaines de mg/L
|
Roches carbonatées (calcaires, dolomies)
|
|
Chlorures (Cl-)
|
Quelques mg/L (la dissolution d'halite ou la présence d'un
biseau salé peut engendrer des valeurs de quelques centaines de mg/L)
|
Origine atmosphérique : dans les aquifères libres,
la concentration en chlorures est directement liée à la teneur en
chlorure des précipitations. Dépend finalement plus de la
distance à la mer que de la lithologie
|
|
Sulfates (SO4-)
|
Quelques mg/L à quelques dizaines de mg/L
(quelques centaines de mg/L dans le cas de lessivage de roches
évaporitiques)
|
Origine atmosphérique (eau de pluie), la mise en solution
de roches sédimentaires évaporitiques, notamment le gypse (CaSO4)
et la pyrite, pollution agricole (engrais)
|
|
Nitrates (NO3-)
|
Inférieure à 5 mg/L pour l'origine naturelle
|
Sources naturelles : précipitations, interactions
sol/végétation Sources anthropiques dès lorsque les
concentrations excèdent 10 mg/L : lessivage d'engrais, rejets
domestiques ou industriels
|
| 

