2.2.4 Causes des
résistances acquises
La cause principale se trouve dans le mauvais usage des
antibiotiques, souvent lorsqu'ils ne sont pas indiqués à des
doses insuffisantes, quelque fois en croyant éliminer un germe alors que
s'en est un autre qui est responsable de l'infection. Des considérations
qui ne sont pas vraiment médicales conduisent trop souvent à
employer le dernier antibiotique connu, favorisant ainsi l'émergence des
germes qui lui seront rapidement résistant alors que d'autres plus
anciens auraient largement suffit (Bimetetal.,
2000 ; Dupeyron, 1997).
2.2.5 résistance
croisée
La résistance croisée fait
référence au spectre d'inactivation liée à un
même mécanisme de résistance vis-à-vis de divers
antibiotiques appartenants à la même famille ou sous-groupe. Cette
notion et utilisée lors de lecture interprétative de
l'antibiogramme. Parmi les nombreux cas de résistances croisées,
des mutations dans les topoisomérases type II, gyrase ou
topoisomérases IV induisent la résistance à l'ensemble des
Fluoroquinolones. Un autre exemple de résistance croisée est
celui de la résistance à la méticilline des staphylocoques
par la production d'une nouvelle PLP2a qui procure également la
résistance aux autres molécules de la famille des â-
lactamines. La conséquence majeure de la résistance
croisée est la sélection croisée. Quant à
laco-résistance, plusieurs mécanismes de résistance
peuvent être associés chez la même bactérie, parfois
stabilisés par intégration dans le chromosome. Chacun des
mécanismes confère par résistance croisée la
résistance à un groupe d'antibiotique conférant à
la bactérie un large spectre de résistance
(Moubarecketal., 2007).
2.2.6 Mécanismes
biochimiques de la résistance
Les mecanismesbiochimiques peuvent être
regroupés en trois grands types de mécanismes Cf (Figure
4) :
v Inactivation
enzymatique
Les résistances par l'inactivation enzymatique de
l'antibiotique : les bêtalactamases (pénicillinases,
céphalosporinases, imipénimases) sont les plus importantes. Ce
sont des enzymes sécrétées notamment par certains
Staphylocoques, Haemophilus, Neisseria et plusieurs
entérobactéries, qui détruisent les antibiotiques à
noyau Bêta-Lactam (Bêta-Lactamines). Signalons au passage que les
pénicillines agissent en empêchant la synthèse du
peptidoglycane, principale constituant de la paroi bactérienne. Il
existe un antagoniste aux bêtalactamases ; l'acide clavulanique
lui-même élaboré par un champignon, Streptomyces
clavuligenus. Cette sécrétion est en générale
naturelle à un taux suffisant pour être efficace. Mais dans
certains cas, la bactérie est naturellement productrice de cette enzyme
à un taux faible, peu efficace. Elle peut subir une augmentation
temporaire de cette sécrétion par le contacte avec un
antibiotique de la famille des bêta-lactamines. C'est le seul cas ou la
résistance est induite par la présence du germe
(Zebaetal., 2007 ; Cambau, 1997). Prenons l'exemple des
ß-lactamines chez un bacille à Gram-négatif, qui pour agir,
doivent traverser la membrane externe ou la paroi au niveau des porines (motif
en bleu ; Figure 8), puis traverser l'espace cytoplasmique et enfin se
fixer sur des cibles ou protéines liant la pénicilline (PLP en
marron : Figure 8) qui sont situées principalement au niveau de la
membrane cytoplasmique. Cette fixation amène à une inhibition de
celles-ci (transpeptidase, transglycosylase....) entraînant des
modifications morphologiques de type filaments (Figure 9) ou au contraire
formes sphéroïdes. Le résultat final est une inhibition de
la synthèse du peptidoglycane (couche interne de la paroi en rose :
avec quelquefois, une lyse finale (Lozniewskia et Rabaud, 2010).
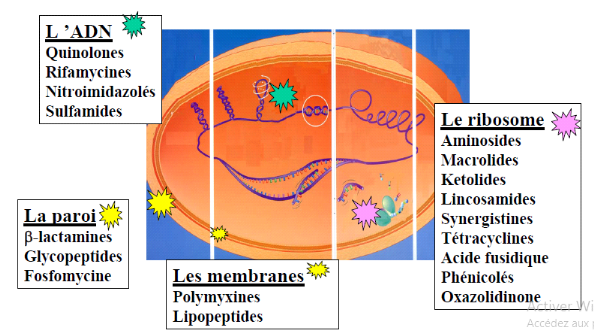
Figure 4 : modification morphologique d'une souche
bactérienne lors d'un traitement par une pénicilline à
large spectre (Philippon, 2004)
| 


