1.5.3. Préparation des échantillons des
selles
La préparation des échantillons des selles a
été spécifiques pour chaque type de selles (selles de
routine). Les fractions des selles d'environ 1 à 1,5 g ont
été prélevées avec de pipette pasteur (en verre) ou
avec une anse de platine stériles et ensemencées directement sur
les milieux ou pour préparer un inoculum. Une fois que l'inoculum est
préparé, les différents milieux sont ensemencés
puis incubés à 37 ° C à l'étuve pendant 24
heures. Après incubation, nous procédons à
l'identification des caractères culturaux et morphologiques des colonies
bactériennes dans ces milieux.
1.5.4. Enrichissement

Le bouillon rappaport (Müller-Kauffmann) a
été utilisé comme milieu d'enrichissement pour l'isolement
des Salmonelles et Shigelles dans les selles. Une fraction de
selles a été prélevée à l'aide d'une anse
à platine et ensemencée dans le tube contenant le bouillon. Le
tube ensemencé a été incubé à 37 ° C
à l'étuve pendant 4 heures au minimum et 24 heures au maximum. Le
bouillon devient trouble lorsque les bactéries l'utilisent. Ensuite une
anse à platine a été trempée dans le bouillon puis
ensemencée dans le milieu Hektoen et incubé à 37 ° C
pendant 24 heures pour la recherche de Salmonella et
Shigella.

Figure 11 :
pré-enrichissement dans RV avant 24h et après 24h.
1.5. Isolement
Le milieu Hektoen a été utilisé comme
milieu d'isolement. Les milieux ensemencés ont été
incubés à 37 ° C à l'étuve pendant 24 heures.
Ensuite, les colonies vertes ou bleuâtres avec ou sans centre noir ont
été recherchées pour l'identification des
Salmonella et Shigella (Figure 19, 20 ; Anexxe
XIII).
Figure 12: RV isolé sur
gélose Kektoen
3.4. Identification des agents
bactériens
3.4.1. Identification biochimique des agents
bactériens
Pour l'identification biochimique des bactéries, les
galeries API® 20E a été utilisé et la
réalisation des antibiogrammes.
ü Les Salmonella, la plupart de
Salmonella isolées (Typhi, para Typhi A, B) ont pour
caractères biochimiques communs : ONPG -, Urée -, TDA -,
Citrate de Simmons -, Indole -. Nous avons remarqué que les
Salmonella Typhi et Salmonella para Typhi B sont souvent
H2S + faible après 24 heures de culture et plus
prononcé 48 heures à 72 heures. Par contre, les
Salmonella para Typhi A isolés ont quelques fois H2S
- après 24 heures de culture, mais, le H2S apparaît
faiblement 72 heures voir une semaine après culture. Elles produisent
des gaz en glucose sauf Salmonella Typhi (Figure 14).
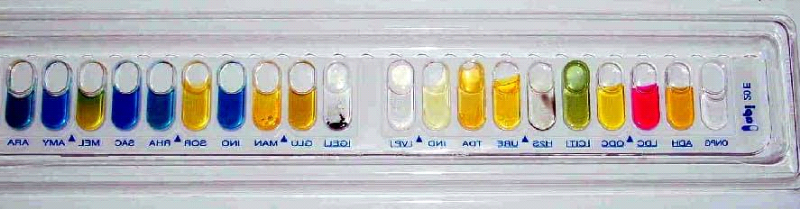
Figure 14 : identification sur galerie API 20 E Salmonella
typhi differenciation biochimique
ü Les Shigella, la majorité des
Shigella isolés ont pour caractères biochimiques
négatifs, mais ils sont tous glucose + (Figure 16), catalase + sauf
Shigella dysenteriae 1est catalase -. L'absence de gaz en glucose est
un indice de suspicion. Les Shigella sont tous immobiles à
l'observation microscopique

Figure 15 : identification sur galerie API 20 E Shigella
flexneri différenciation biochimique
Tableau VIII :
caractères biochimiques différentiels des
entérobactéries pathogènes
|
Caractères différentiels des
entérobactéries
|
Glucose
|
Lactose
|
ONPG
|
Uréase
|
TDA
|
Mobilité
|
Mannitol
|
Indole
|
VP
|
H2S
|
|
Salmonella Typhi
Salmonella para Typhi A
Salmonella para Typhi B
Salmonella para Typhi C
Salmonella Typhimurium
Salmonella enteritidis
|
+
+
+
+
+
+
|
-
-
-
-
-
-
|
-
-
-
-
-
-
|
-
-
-
-
-
-
|
-
-
-
-
-
-
|
+
+
+
+
+
+
|
+
+
+
+
+
+
|
-
-
-
-
-
-
|
-
-
-
-
-
-
|
(+)
(-)
+
+
+
(+)
|
|
Shigella dysenteriae 1
Shigella flexneri
Shigella sonnei
Shigellaboydii
|
+
+
+
+
|
-
-
(+) lent
-
|
(+)
(+)
(+)
(+)
|
-
-
-
-
|
-
-
-
-
|
-
-
-
-
|
-
(+)
+
+
|
(+)
(-)
-
-
|
-
-
-
-
|
-
-
-
-
|
NB : (+) et (-) sont des
caractères biochimiques variables
| 


