C.1- Présentation
Les anthocyanes (du grec anthos, fleur et Kuanos, bleu violet)
terme général qui regroupe les anthocyanidols et leurs
dérivés glycosylés [Guignard, 1996]. Ces
molécules faisant partie de la famille des flavonoïdes et capables
d'absorber la lumière visible, sont des pigments qui colorent les
plantes en bleu, rouge, mauve, rose ou orange [Harborne., 1967.
Brouillard., 1986].
Leur présence dans les plantes est donc
détectable à l'oeil nu. A l'origine de la couleur des fleurs, des
fruits et des bais rouges ou bleues, elles sont généralement
localisées dans les vacuoles des cellules épidermiques, qui sont
de véritables poches remplis d'eau [Mclure, 1979; Harbone et
Grayer, 1988; Merlin et al., 1985].
Si la coloration des fleurs et des fruits est leur rôle
le plus connu, on trouve également les anthocynes dans les racines,
tiges, feuilles et graines. En automne, les couleurs caractéristiques
des feuilles des arbres sont du aux anthocyanes et aux carotènes qui ne
sont plus masqués par la chlorophylle.
C.2- Structures
Leur structure de base est caractérisée par un
noyau "flavon" généralement glucosylé en position C3
[Ribereau, 1968]. Les anthocyanes se différencient par
leur degré d'hydroxylation et de méthylation, par la nature, le
nombre et la position des oses liés à la molécule.
L'aglycone ou anthocyanidine constitue le groupement chromophore du pigment
(Fig. 07).
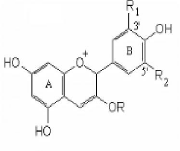
|
Anthocyanidines
R=H
|
R1
|
R2
|
|
Malvidine
|
OCH3
|
OCH3
|
|
Péonidine
|
OCH3
|
H
|
|
Delphinidine
|
OH
|
OH
|
|
Pétunidine
|
OCH3
|
OH
|
Si la forme est monoglucoside: R= glucose
Figure. 07: Structure de quelques anthocyanidine
[Ribereau., 1968].
C.3- Propriétés des anthocyanes
+ Le spectre d'absorption : Comme tous les
flavonoides, les anthocyanidines présentent une absorption
caractéristique dans le domaine UV [Markham, 1982]. La forme cationique
de l'anthocyanidine est caractérisée par deux bandes
d'absorption, dont une bande intense dans le domaine du visible,
caractéristique pour chacune d'ente elles [Harbone, 1967]. Ce maximum
d'absorption subi un effet bathochrome quand la polarité des solvants
diminue (solvatochromie négative), par contre on observe un effet
hypsochrome quand les positions 3' et 5' sont méthoxylées ou
glycosylées. Les sucres augmentent la solubilité et la
stabilité des anthocyanes.
+ Modification de la structure en fonction de
l'acidité : Le pH est un facteur important dans le changement
de couleur des anthocyanes. La variation de structure de l'anthocyane en
fonction du pH est une particularité de ces molécules. Les
observations visuelles d'une solution aqueuse d'anthocyane montrent la forte
coloration rouge d'une solution à pH très acide, la coloration
décroît quand le pH augmente vers la neutralité. Une
solution neutre d'anthocyane fraîchement préparée est bleue
mais se décolore rapidement.
Ces changement de couleurs sont dus à des
équilibres chimiques entre différentes formes que peut prendre
l'anthocyane [Brouillard et Delaporte, 1977; Brouillard,
1982].
+ Décoloration par le Bisulfite de Sodium
: La décoloration des anthocyanes par l'acide sulfureux et les
bisulfites alcalins est une réaction connue depuis longtemps. Cette
réaction se fait mieux à pH 3 qu'à pH 1. D'autre part la
réaction est réversible mais uniquement dans le cas des
anthocyanines. La difficulté de la réaction en milieux acide
s'explique par le passage du bisulfite sous forme d'acide sulfureux moins
dissocié, avec diminution de la concentration en ions HSO3
[Ribéreau, 1968].
| 


